PharmaCon 2019第五届中国国际化学药研发论坛
中国加入ICH标志着我国药品标准在国际合作领域迈出重要的一步。为着力推进ICH 指导原则在中国的转化实施,我国实施了MAH药品上市许可持有人制度,积极推进仿制药质量和疗效一致性评价,同时也颁布了注射剂一致性评价技术要求,原辅包关联审评等一系列法规,企业面临着政策该如何落地的困局,故而行业亟待一个平台来探讨推进。
随着我国医药行业的快速发展,“4+7“带量采购等一系列政策鼓励药物双创,促进新药研发成果转化和生产。随着未来药品获批上市数量的增多,改良制剂与高端制剂的市场空前巨大。因此加强改良制剂和高端制剂的研发迫在眉睫。目前难溶片剂、缓控释制剂与新载体制剂的研发面临着如何增加临床有效性、提高生产工艺稳定性以及产业化发展仍存在诸多阶段性挑战。
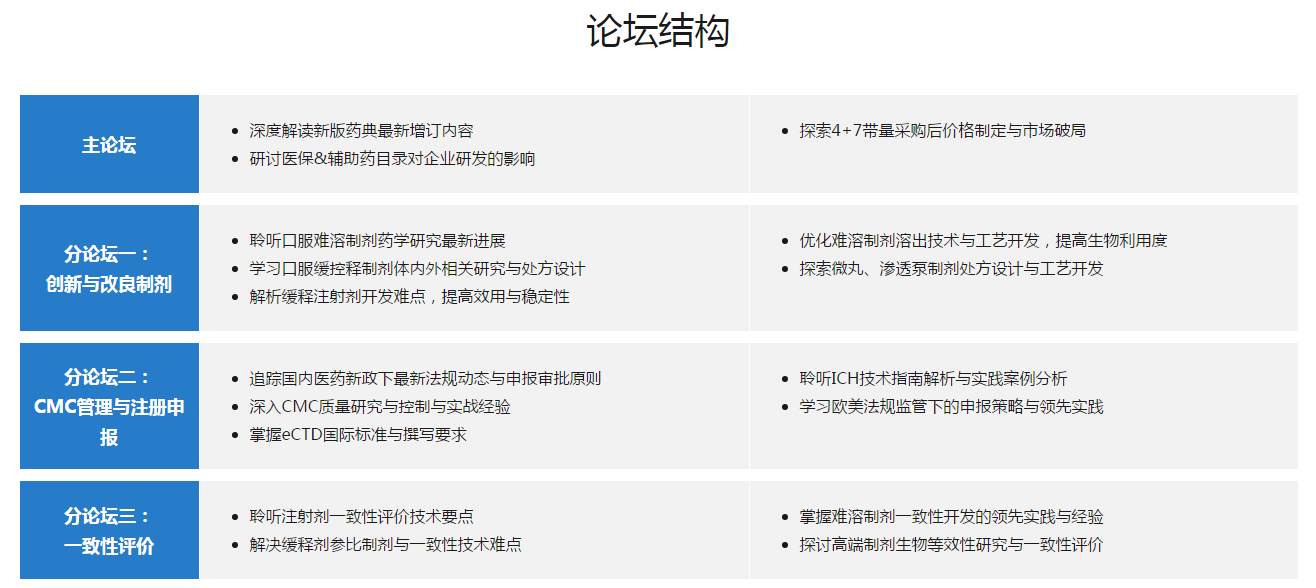
在此背景下,PharmaCon组委会作为中国化药企业最为顶尖的会议平台,致力于促进整体行业的交流与进步。PharmaCon2019第五届中国国际化学药研发论坛将汇聚600多位国内外领先的化学药企业以及药品监管机构官员的领导人,共同探索国家政策、创新与改良制剂、CMC管理与注册申报、一致性评价中药企面临的共同难题与挑战。四大板块将为众企业提供最前沿,最有价值的交流机会。
PharmaCon 2019 期待您的莅临!
重要会议时间
会议时间 2019-09-24 08:30 ~ 09-25 17:30
会议地点
上海徐汇区上海富豪环球东亚酒店
参会群体
化药企业:制剂部、法规注册部、工艺开发部、质量分析部等
药品注册及监管机构法规专家
临床试验研究者、数据管理人员、项目管理人员等
CRO以及技术设备的高级管理人员
联系组委会
电话:+86 18017939885
邮箱:pharmacon@bmapglobal.com
凡文章来源标注为 “ 晟斯医学 ” ,则是本站原创编译整理,未经本网站授权不得转载和使用。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
- 2019诺贝尔奖获得者医学峰会(成都)
- PharmaCon 2019第五届中国国际化学药研发论坛
- ATBP2019第三届抗体药物开发暨工艺技术论坛(上海)
- 2019第二届国际合成生物学论坛(SynBioForum 2019 南京)
- PDI2019第十二届注射剂工业大会
- 2019年临床药学学术年会通知
- The 11th International Conference on Supercritical Fluids-Supergreen 2019
- 长江药学之路2019年学术会议
- 2019第八届特殊医学用途配方食品高峰论坛暨注册申报、临床应用与技术评审创新大会(泰州)
- 重庆市医学会2019年临床药学学术年会